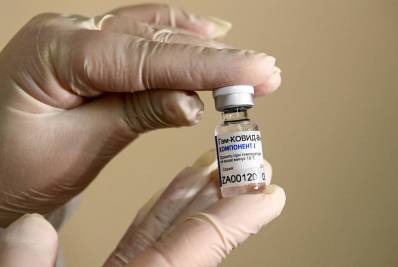
Espera-se que a Pfizer/BioNTech e a Moderna solicitem autorizações de comercialização dos Estados Unidos, Europa e outras autoridades nas próximas semanas.
Complexidade europeia
A Moderna, que desenvolveu seu medicamento em parceria com o National Institutes of Health (CDC) dos Estados Unidos, já assinou acordos para fornecer a vacina para Canadá, Japão, Israel, Catar e Reino Unido. Agora espera pela União Europeia.
"Existem muitas coisas administrativas, os arquivos, os sigilos, os alinhamentos entre os países e é difícil administrar isso quando você tem 27 (os membros da UE) em comparação com quando é apenas um", explicou Bancel.
Nesse sentido, ele comparou ao Canadá: entre as primeiras conversas com os médicos da Moderna e a assinatura do contrato, "demorou duas semanas" apenas para finalizar o acordo.
Para todos os países, exceto os Estados Unidos, a produção será realizada na Suíça, nas fábricas do grupo Lonza, e o envazamento em Madri, no grupo Rovi.
Se em algum momento a Agência Europeia de Medicamentos autorizar a vacina antes do final do ano, "as primeiras entregas não incluirão a UE. Iriam para Suíça, Japão, Israel, Canadá, países que já fizeram o pedido. Para os que não pediram, não mandaremos produtos".
"Quanto mais eles esperarem, mais demorará a entrega", insistiu o CEO da Moderna.
Segundo ele, as discussões não estão bloqueadas pelo preço, mas ele se recusa a falar o motivo publicamente.
A Comissão Europeia, que assinou com a Pfizer e outros fabricantes, insistiu nesta terça-feira sobre a complexidade das negociações.
"Vamos fechar negócios porque, de repente, há algumas boas notícias na imprensa sobre o status desta vacina? Claramente, não é o caso", disse Stefan, porta-voz da Keersmaecker.
Antecipação dos EUA
À lentidão europeia se contrapõe a antecipação americana. Desde 2 de março, CEO da Moderna e dos principais laboratórios estiveram na Casa Branca junto com o presidente republicano Donald Trump para negociações.
Os Estados Unidos prometeram 500 milhões de dólares à Moderna em abril para financiar testes clínicos. No total, a empresa de biotecnologia recebeu 2,5 bilhões do tesouro público dos Estados Unidos, sob os auspícios da Operação Warp Speed, lançada oficialmente em 15 de maio.
"A Operação Warp Speed foi uma das coisas mais eficazes", disse o chefe da Moderna.
"Começamos a conversar com vários países europeus em maio. Não conseguimos ajuda para pagar nenhum estudo clínico. Tudo foi assumido pelo governo dos Estados Unidos e felizmente eles concretizaram, caso contrário não teríamos feito", disse.
Segundo Bancel, se não fosse pelos Estados Unidos "a vacina não poderia ter sido desenvolvida a essa velocidade". "Como sabem, somos uma empresa que nunca teve lucro em euros, e o estudo clínico custou mil milhões de dólares", explicou.
O resultado é que os primeiros americanos serão vacinados antes do Ano Novo e milhões de doses já estão em estoque. Devem estar disponíveis dez milhões de doses até o final de novembro e haverá "20 milhões de doses até o final do ano", disse.
As 20 milhões de doses serão destinadas exclusivamente aos Estados Unidos. A Moderna vem preparando a cadeia de suprimentos com o governo dos EUA há meses para estar pronta para distribuição assim que a Food and Drug Administration (FDA) dos EUA aprovar a vacina, uma decisão esperada em dezembro.
O objetivo, segundo Bancel, é que assim que o sinal verde do FDA sair, a Moderna possa "carregar os caminhões e ir" distribuir.